Հեղինակ:
Mark Sanchez
Ստեղծման Ամսաթիվը:
3 Հունվար 2021
Թարմացման Ամսաթիվը:
1 Հուլիս 2024

Բովանդակություն
- Քայլեր
- Մեթոդ 1 2 -ից. Massանգվածի տոկոսադրույքի որոշում `հիմնված նշված քաշերի վրա
- Մեթոդ 2 2 -ից. Massանգվածի տոկոսադրույքի որոշում, երբ զանգվածներ չեն նշվում
Percentանգվածային տոկոսը սահմանում է քիմիական միացության տարրերի տոկոսը: Massանգվածի տոկոսը գտնելու համար հարկավոր է իմանալ բաղադրության մեջ մտնող տարրերի մոլային զանգվածը (գրամում մեկ մոլի վրա) կամ յուրաքանչյուր լուծույթի ստացման համար անհրաժեշտ յուրաքանչյուր բաղադրիչի գրամի քանակը:Massանգվածի տոկոսը հաշվարկվում է բավականին պարզ ՝ բավական է տարրի (կամ բաղադրիչի) զանգվածը բաժանել ամբողջ միացության (կամ լուծույթի) զանգվածի վրա:
Քայլեր
Մեթոդ 1 2 -ից. Massանգվածի տոկոսադրույքի որոշում `հիմնված նշված քաշերի վրա
 1 Քիմիական միացության քաշի տոկոսը որոշելու համար ընտրեք հավասարություն: Massանգվածի տոկոսը հաշվարկվում է հետևյալ բանաձևի միջոցով. Զանգվածային տոկոս = (բաղադրիչի զանգվածը / բաղադրության ընդհանուր զանգվածը) x 100. Տոկոս ստանալու համար բաժանման արդյունքը բազմապատկվում է 100 -ով:
1 Քիմիական միացության քաշի տոկոսը որոշելու համար ընտրեք հավասարություն: Massանգվածի տոկոսը հաշվարկվում է հետևյալ բանաձևի միջոցով. Զանգվածային տոկոս = (բաղադրիչի զանգվածը / բաղադրության ընդհանուր զանգվածը) x 100. Տոկոս ստանալու համար բաժանման արդյունքը բազմապատկվում է 100 -ով: - Խնդրի լուծման սկզբում գրեք հավասարությունը. զանգվածային տոկոս = (բաղադրիչի զանգվածը / բաղադրության ընդհանուր զանգվածը) x 100.
- Ձեզ հետաքրքրող բաղադրիչի զանգվածը պետք է լինի խնդրի վիճակում: Եթե ոչ մի զանգված չի տրվում, անցեք հաջորդ բաժին, որը բացատրում է, թե ինչպես որոշել զանգվածի տոկոսը անհայտ զանգվածով:
- Քիմիական միացության ընդհանուր զանգվածը հայտնաբերվում է այս միացության (կամ լուծույթի) մաս կազմող բոլոր տարրերի (բաղադրիչների) զանգվածները ավելացնելով:
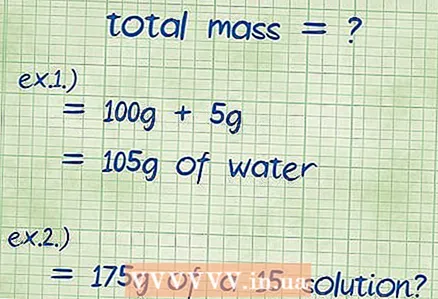 2 Հաշվիր միացության ընդհանուր զանգվածը: Եթե գիտեք միացությունը կազմող բոլոր բաղադրիչների զանգվածները, ապա պարզապես ավելացրեք դրանք, և այս կերպ դուք կգտնեք ստացված միացության կամ լուծույթի ընդհանուր զանգվածը: Դուք օգտագործում եք այս զանգվածը որպես հայտարարիչ զանգվածի տոկոսային հարաբերակցության համար:
2 Հաշվիր միացության ընդհանուր զանգվածը: Եթե գիտեք միացությունը կազմող բոլոր բաղադրիչների զանգվածները, ապա պարզապես ավելացրեք դրանք, և այս կերպ դուք կգտնեք ստացված միացության կամ լուծույթի ընդհանուր զանգվածը: Դուք օգտագործում եք այս զանգվածը որպես հայտարարիչ զանգվածի տոկոսային հարաբերակցության համար: - Օրինակ 1: Որքա՞ն է 100 գրամ ջրում լուծված 5 գրամ նատրիումի հիդրօքսիդի զանգվածային տոկոսը:
- Լուծույթի ընդհանուր զանգվածը հավասար է նատրիումի հիդրօքսիդի և ջրի գումարի գումարին. 100 գ + 5 գ տալիս է 105 գ:
- Օրինակ 2: Որքա՞ն նատրիումի քլորիդ և ջուր է անհրաժեշտ 15 տոկոսանոց լուծույթի 175 գրամ պատրաստելու համար:
- Այս օրինակում տրված է ընդհանուր զանգվածը և պահանջվող տոկոսը, և պահանջվում է գտնել նյութի այն քանակությունը, որը պետք է ավելացնել լուծույթին: Ընդհանուր քաշը `175 գրամ:
- Օրինակ 1: Որքա՞ն է 100 գրամ ջրում լուծված 5 գրամ նատրիումի հիդրօքսիդի զանգվածային տոկոսը:
 3 Որոշեք նշված բաղադրիչի զանգվածը: Եթե ձեզ խնդրեն հաշվարկել «զանգվածային տոկոսը», ապա պետք է պարզեք, թե նյութի ընդհանուր զանգվածի քանի տոկոսն է որոշակի բաղադրիչի զանգվածը: Գրանցեք նշված բաղադրիչի զանգվածը: Սա կլինի զանգվածի տոկոսի բանաձևի համարիչը:
3 Որոշեք նշված բաղադրիչի զանգվածը: Եթե ձեզ խնդրեն հաշվարկել «զանգվածային տոկոսը», ապա պետք է պարզեք, թե նյութի ընդհանուր զանգվածի քանի տոկոսն է որոշակի բաղադրիչի զանգվածը: Գրանցեք նշված բաղադրիչի զանգվածը: Սա կլինի զանգվածի տոկոսի բանաձևի համարիչը: - Օրինակ 1. Տրված բաղադրիչի `նատրիումի հիդրոքլորիդի զանգվածը 5 գրամ է:
- Օրինակ 2. Այս օրինակում տվյալ բաղադրիչի զանգվածը անհայտ է և պետք է գտնվի:
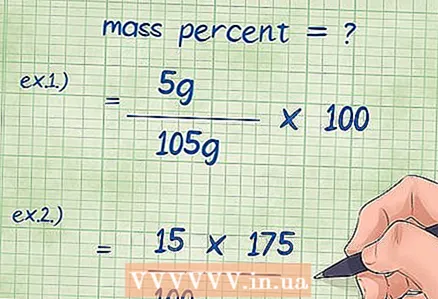 4 Միացրեք արժեքները զանգվածի տոկոսային հավասարման մեջ: Բոլոր անհրաժեշտ արժեքները որոշելուց հետո դրանք միացրեք բանաձևին:
4 Միացրեք արժեքները զանգվածի տոկոսային հավասարման մեջ: Բոլոր անհրաժեշտ արժեքները որոշելուց հետո դրանք միացրեք բանաձևին: - Օրինակ 1. Զանգվածային տոկոս = (բաղադրիչի զանգվածը / բաղադրության ընդհանուր զանգվածը) x 100 = (5 գ / 105 գ) x 100:
- Օրինակ 2. Անհրաժեշտ է փոխակերպել զանգվածի տոկոսային բանաձևը, որպեսզի քիմիական բաղադրիչի անհայտ զանգվածը գտնվի. Բաղադրիչի զանգվածը = (զանգվածի տոկոսը * բաղադրության ընդհանուր զանգվածը) / 100 = (15 * 175) / 100:
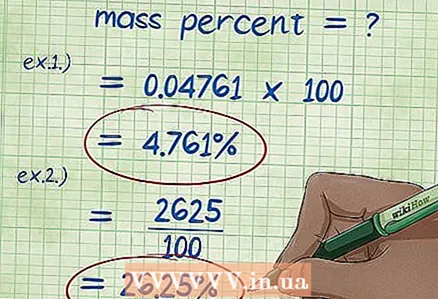 5 Հաշվիր զանգվածի տոկոսը: Բանաձևի բոլոր արժեքները զանգվածի տոկոսը փոխարինելուց հետո կատարեք անհրաժեշտ հաշվարկները: Բաժանեք բաղադրիչի զանգվածը քիմիական միացության կամ լուծույթի ընդհանուր քաշի վրա և բազմապատկեք 100 -ով: Արդյունքն այդ բաղադրիչի զանգվածային տոկոսն է:
5 Հաշվիր զանգվածի տոկոսը: Բանաձևի բոլոր արժեքները զանգվածի տոկոսը փոխարինելուց հետո կատարեք անհրաժեշտ հաշվարկները: Բաժանեք բաղադրիչի զանգվածը քիմիական միացության կամ լուծույթի ընդհանուր քաշի վրա և բազմապատկեք 100 -ով: Արդյունքն այդ բաղադրիչի զանգվածային տոկոսն է: - Օրինակ 1 ՝ (5/105) x 100 = 0.04761 x 100 = 4.761%: Այսպիսով, 100 գրամ ջրում լուծված 5 գրամ նատրիումի հիդրոքլորիդի քաշային տոկոսը կազմում է 4,761%:
- Օրինակ 2. Բաղադրիչի զանգվածային տոկոսի համար վերաշարադրված արտահայտությունն է (զանգվածի տոկոսը * նյութի ընդհանուր զանգվածը) / 100, որից մենք գտնում ենք. (15 * 175) / 100 = (2625) / 100 = 26.25 գրամ նատրիումի քլորիդ:
- Մենք գտնում ենք ջրի անհրաժեշտ քանակությունը `լուծույթի ընդհանուր զանգվածից հանելով բաղադրիչի զանգվածը` 175 - 26,25 = 148,75 գրամ ջուր:
Մեթոդ 2 2 -ից. Massանգվածի տոկոսադրույքի որոշում, երբ զանգվածներ չեն նշվում
 1 Ընտրեք բանաձև քիմիական միացության քաշի տոկոսի համար: Massանգվածային տոկոս գտնելու հիմնական հավասարումը հետևյալն է. Զանգվածային տոկոս = (տարրի մոլային զանգված / միացության ընդհանուր մոլեկուլային զանգված) x 100. Նյութի մոլային զանգվածը տվյալ նյութի մեկ մոլի զանգվածն է, մինչդեռ մոլեկուլային զանգվածը ամբողջ քիմիական նյութի մեկ մոլի զանգվածն է: կապերը: Տոկոսները ստանալու համար բաժանումը բազմապատկվում է 100 -ով:
1 Ընտրեք բանաձև քիմիական միացության քաշի տոկոսի համար: Massանգվածային տոկոս գտնելու հիմնական հավասարումը հետևյալն է. Զանգվածային տոկոս = (տարրի մոլային զանգված / միացության ընդհանուր մոլեկուլային զանգված) x 100. Նյութի մոլային զանգվածը տվյալ նյութի մեկ մոլի զանգվածն է, մինչդեռ մոլեկուլային զանգվածը ամբողջ քիմիական նյութի մեկ մոլի զանգվածն է: կապերը: Տոկոսները ստանալու համար բաժանումը բազմապատկվում է 100 -ով: - Խնդրի լուծման սկզբում գրեք հավասարությունը. զանգվածային տոկոս = (տարրի մոլային զանգված / բաղադրության ընդհանուր մոլեկուլային զանգված) x 100.
- Երկու քանակներն էլ չափվում են գրամով մեկ մոլի համար (գ / մոլ):
- Եթե ձեզ զանգվածներ չեն տրվում, տվյալ նյութի տարրի զանգվածի տոկոսը կարելի է գտնել մոլային զանգվածի միջոցով:
- Օրինակ 1: Գտեք ջրածնի զանգվածային տոկոսը ջրի մոլեկուլում:
- Օրինակ 2: Գտեք գլյուկոզայի մոլեկուլում ածխածնի զանգվածային տոկոսը:
 2 Գրեք քիմիական բանաձևը: Եթե օրինակը չի տալիս նշված նյութերի քիմիական բանաձևերը, ապա դրանք ինքներդ պետք է գրեք: Եթե առաջադրանքը պարունակում է քիմիական նյութերի համար անհրաժեշտ բանաձևեր, կարող եք բաց թողնել այս քայլը և անմիջապես անցնել հաջորդ քայլին (գտնել յուրաքանչյուր տարրի զանգվածը):
2 Գրեք քիմիական բանաձևը: Եթե օրինակը չի տալիս նշված նյութերի քիմիական բանաձևերը, ապա դրանք ինքներդ պետք է գրեք: Եթե առաջադրանքը պարունակում է քիմիական նյութերի համար անհրաժեշտ բանաձևեր, կարող եք բաց թողնել այս քայլը և անմիջապես անցնել հաջորդ քայլին (գտնել յուրաքանչյուր տարրի զանգվածը): - Օրինակ 1. Գրեք ջրի քիմիական բանաձևը, H2Օ.
- Օրինակ 2. Գրեք գլյուկոզայի քիմիական բանաձևը, C6Հ12Օ6.
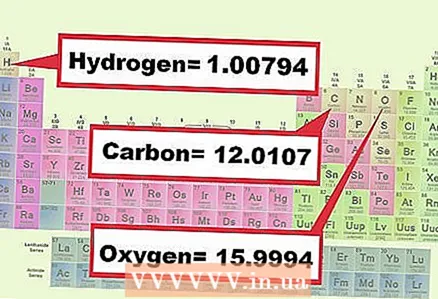 3 Գտեք բաղադրության յուրաքանչյուր տարրի զանգվածը: Որոշեք քիմիական բանաձևի յուրաքանչյուր տարրի մոլային քաշը `ըստ պարբերական համակարգի: Սովորաբար, տարրի զանգվածը նշված է նրա քիմիական նշանի տակ: Գրեք խնդրո առարկա միացությունը կազմող բոլոր տարրերի մոլային զանգվածները:
3 Գտեք բաղադրության յուրաքանչյուր տարրի զանգվածը: Որոշեք քիմիական բանաձևի յուրաքանչյուր տարրի մոլային քաշը `ըստ պարբերական համակարգի: Սովորաբար, տարրի զանգվածը նշված է նրա քիմիական նշանի տակ: Գրեք խնդրո առարկա միացությունը կազմող բոլոր տարրերի մոլային զանգվածները: - Օրինակ 1. Գտեք թթվածնի (15.9994) և ջրածնի (1.0079) մոլային զանգվածները:
- Օրինակ 2. Գտեք ածխածնի (12.0107), թթվածնի (15.9994) և ջրածնի (1.0079) մոլային զանգվածները:
 4 Բազմապատկեք յուրաքանչյուր տարրի մոլային զանգվածը նրա մոլային բաժնի միջոցով: Որոշեք, թե յուրաքանչյուր տարրից քանի մոլ է պարունակվում տվյալ քիմիական նյութում, այսինքն ՝ տարրերի մոլի ֆրակցիաները: Մոլի կոտորակները տրվում են բանաձևի տարրերի խորհրդանիշների ներքևի թվերով: Բազմապատկեք յուրաքանչյուր տարրի մոլային զանգվածը նրա մոլային բաժնի միջոցով:
4 Բազմապատկեք յուրաքանչյուր տարրի մոլային զանգվածը նրա մոլային բաժնի միջոցով: Որոշեք, թե յուրաքանչյուր տարրից քանի մոլ է պարունակվում տվյալ քիմիական նյութում, այսինքն ՝ տարրերի մոլի ֆրակցիաները: Մոլի կոտորակները տրվում են բանաձևի տարրերի խորհրդանիշների ներքևի թվերով: Բազմապատկեք յուրաքանչյուր տարրի մոլային զանգվածը նրա մոլային բաժնի միջոցով: - Օրինակ 1 ՝ ջրածնի խորհրդանիշի տակ կա 2, իսկ թթվածնի խորհրդանիշի տակ ՝ 1 (համարի բացակայությանը համարժեք): Այսպիսով, ջրածնի մոլային զանգվածը պետք է բազմապատկվի 2 -ով `1.00794 X 2 = 2.01588; թթվածնի մոլային զանգվածը թողնում ենք նույնը ՝ 15.9994 (այսինքն ՝ բազմապատկում 1 -ով):
- Օրինակ 2. Ածխածնի խորհրդանիշի տակ կա 6, ջրածնի տակ ՝ 12 և թթվածնի տակ ՝ 6. Թվերի տարրերի մոլային զանգվածները բազմապատկելով այս թվերով ՝ գտնում ենք.
- ածխածին `(12.0107 * 6) = 72.0642
- ջրածին ՝ (1.00794 * 12) = 12.09528
- թթվածին `(15.9994 * 6) = 95.9964
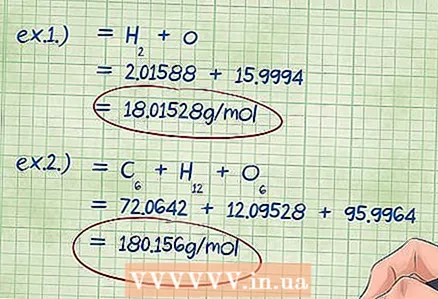 5 Հաշվիր միացության ընդհանուր զանգվածը: Ավելացրեք այս բաղադրության մեջ ներառված բոլոր տարրերի հայտնաբերված զանգվածները: Մոլային կոտորակներով տարրերի մոլային զանգվածների գումարը ձեզ կստանա քիմիական միացության ընդհանուր զանգվածը: Այս թիվը զանգվածի տոկոսի բանաձևի բաժանարարն է:
5 Հաշվիր միացության ընդհանուր զանգվածը: Ավելացրեք այս բաղադրության մեջ ներառված բոլոր տարրերի հայտնաբերված զանգվածները: Մոլային կոտորակներով տարրերի մոլային զանգվածների գումարը ձեզ կստանա քիմիական միացության ընդհանուր զանգվածը: Այս թիվը զանգվածի տոկոսի բանաձևի բաժանարարն է: - Օրինակ 1. Ավելացնել 2,01588 գ / մոլ (ջրածնի ատոմների երկու մոլի զանգված) 15,9994 գ / մոլ (թթվածնի ատոմների մեկ մոլի զանգվածը), արդյունքը ՝ 18,01528 գ / մոլ:
- Օրինակ 2. Ավելացրեք գտնված մոլային զանգվածները ՝ ածխածին + ջրածին + թթվածին = 72.0642 + 12.09528 + 95.9964 = 180.156 գ / մոլ:
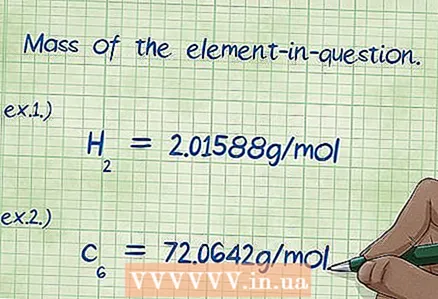 6 Որոշեք հետաքրքրության տարրի զանգվածը: Եթե ձեզ խնդրեն գտնել «զանգվածի տոկոսը», ապա դուք պետք է հաշվարկեք բաղադրության մաս կազմող որոշակի տարրի զանգվածը ՝ որպես բոլոր տարրերի ընդհանուր զանգվածի տոկոս: Գտեք տրված տարրի զանգվածը և գրեք այն: Դա անելու համար անհրաժեշտ է բազմապատկել տարրի մոլային զանգվածը նրա մոլային բաժնով: Արդյունքում, զանգվածի տոկոսի բանաձևի համարիչում ստանում եք արժեքը:
6 Որոշեք հետաքրքրության տարրի զանգվածը: Եթե ձեզ խնդրեն գտնել «զանգվածի տոկոսը», ապա դուք պետք է հաշվարկեք բաղադրության մաս կազմող որոշակի տարրի զանգվածը ՝ որպես բոլոր տարրերի ընդհանուր զանգվածի տոկոս: Գտեք տրված տարրի զանգվածը և գրեք այն: Դա անելու համար անհրաժեշտ է բազմապատկել տարրի մոլային զանգվածը նրա մոլային բաժնով: Արդյունքում, զանգվածի տոկոսի բանաձևի համարիչում ստանում եք արժեքը: - Օրինակ 1. Միացության մեջ ջրածնի զանգվածը կազմում է 2.01588 գ / մոլ (ջրածնի ատոմների երկու մոլի զանգվածը):
- Օրինակ 2. Միացության մեջ ածխածնի զանգվածը 72.0642 գ / մոլ է (ածխածնի ատոմների վեց մոլի զանգվածը):
 7 Փոխարինեք թվային արժեքները զանգվածի տոկոսային հավասարման մեջ: Բոլոր մեծությունների արժեքները որոշելուց հետո դրանք միացրեք առաջին քայլին տրված բանաձևին. Զանգվածի տոկոս = = (տարրի մոլային զանգված / միացության ընդհանուր մոլեկուլային զանգված) x 100:
7 Փոխարինեք թվային արժեքները զանգվածի տոկոսային հավասարման մեջ: Բոլոր մեծությունների արժեքները որոշելուց հետո դրանք միացրեք առաջին քայլին տրված բանաձևին. Զանգվածի տոկոս = = (տարրի մոլային զանգված / միացության ընդհանուր մոլեկուլային զանգված) x 100: - Օրինակ 1. Զանգվածային տոկոս = (տարրի մոլային զանգված / բաղադրության ընդհանուր մոլեկուլային զանգված) x 100 = (2.01588 / 18.01528) x 100:
- Օրինակ 2. զանգվածային տոկոս = (տարրի մոլային զանգված / բաղադրության ընդհանուր մոլեկուլային զանգված) x 100 = (72.0642 / 180.156) x 100:
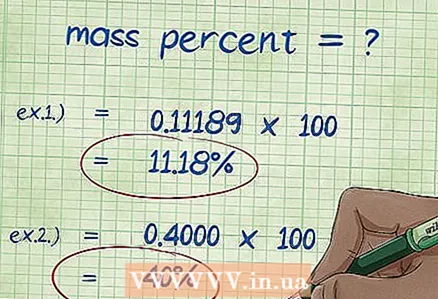 8 Հաշվիր զանգվածի տոկոսը: Թվային արժեքները փոխարինելուց հետո կատարեք անհրաժեշտ թվաբանական գործողությունները:Տարրի զանգվածը բաժանել միացության ընդհանուր զանգվածի վրա և բազմապատկել 100 -ով: Արդյունքում ստացվում է տարրի զանգվածային տոկոսը:
8 Հաշվիր զանգվածի տոկոսը: Թվային արժեքները փոխարինելուց հետո կատարեք անհրաժեշտ թվաբանական գործողությունները:Տարրի զանգվածը բաժանել միացության ընդհանուր զանգվածի վրա և բազմապատկել 100 -ով: Արդյունքում ստացվում է տարրի զանգվածային տոկոսը: - Օրինակ 1. Զանգվածային տոկոս = (տարրի մոլային զանգված / բաղադրության ընդհանուր մոլեկուլային զանգված) x 100 = (2.01588 / 18.01528) x 100 = 0.111189 x 100 = 11.18%: Այսպիսով, ջրածնի ատոմների զանգվածային տոկոսը ջրի մոլեկուլում կազմում է 11,18%:
- Օրինակ 2. զանգվածային տոկոս = (տարրի մոլային զանգված / բաղադրության ընդհանուր մոլեկուլային զանգված) x 100 = (72.0642 / 180.156) x 100 = 0.4000 x 100 = 40.00%: Այսպիսով, գլյուկոզայի մոլեկուլում ածխածնի ատոմների քաշային տոկոսը 40,00%է: