Հեղինակ:
Clyde Lopez
Ստեղծման Ամսաթիվը:
26 Հուլիս 2021
Թարմացման Ամսաթիվը:
1 Հուլիս 2024

Բովանդակություն
- Քայլեր
- Մեթոդ 1 4 -ից. Տոկոսի հաշվարկ քաշի / ծավալի բանաձևի միջոցով
- Մեթոդ 2 4 -ից ՝ մոլեկուլային լուծույթի պատրաստում
- Մեթոդ 3 4 -ից. Հայտնի կոնցենտրացիայի լուծույթների լուծում
- Մեթոդ 4 -ից 4 -ը. Համապատասխանություն անվտանգության նախազգուշական միջոցներին
- Խորհուրդներ
- Գուշացումներ
- Ինչ է պետք
Քիմիական պարզ լուծումները կարող են հեշտությամբ պատրաստվել տարբեր եղանակներով ՝ տանը կամ աշխատավայրում: Անկախ նրանից, թե փոշոտ նյութից լուծում եք պատրաստում կամ հեղուկ եք նոսրացնում, հեշտ է որոշել յուրաքանչյուր բաղադրիչի ճիշտ քանակությունը: Քիմիական լուծումներ պատրաստելիս հիշեք, որ օգտագործեք անձնական պաշտպանիչ սարքավորումներ `վնասներից խուսափելու համար:
Քայլեր
Մեթոդ 1 4 -ից. Տոկոսի հաշվարկ քաշի / ծավալի բանաձևի միջոցով
 1 Սահմանել տոկոսը բովանդակությունը միացված է քաշը/ լուծույթի ծավալը: Տոկոսները ցույց են տալիս, թե նյութի քանի մաս կա լուծույթի հարյուր մասում: Քիմիական լուծույթների կիրառման դեպքում դա նշանակում է, որ եթե կոնցենտրացիան 1 տոկոս է, ապա 100 միլիլիտր լուծույթը պարունակում է 1 գրամ նյութ, այսինքն ՝ 1 մլ / 100 մլ:
1 Սահմանել տոկոսը բովանդակությունը միացված է քաշը/ լուծույթի ծավալը: Տոկոսները ցույց են տալիս, թե նյութի քանի մաս կա լուծույթի հարյուր մասում: Քիմիական լուծույթների կիրառման դեպքում դա նշանակում է, որ եթե կոնցենտրացիան 1 տոկոս է, ապա 100 միլիլիտր լուծույթը պարունակում է 1 գրամ նյութ, այսինքն ՝ 1 մլ / 100 մլ: - Օրինակ ՝ ըստ քաշի. 10% քաշային լուծույթը պարունակում է 10 գրամ նյութ, որը լուծարված է 100 միլիլիտր լուծույթում:
- Օրինակ ՝ ըստ ծավալի. 23 տոկոս ծավալով լուծույթը պարունակում է 23 միլիլիտր հեղուկ միացություն յուրաքանչյուր 100 միլիլիտր լուծույթի մեջ:
 2 Որոշեք լուծման ծավալը, որը ցանկանում եք պատրաստել: Նյութի պահանջվող զանգվածը պարզելու համար նախ պետք է որոշեք ձեզ անհրաժեշտ լուծույթի վերջնական ծավալը: Այս ծավալը կախված է նրանից, թե որքան լուծում է անհրաժեշտ, որքան հաճախ եք այն օգտագործելու և պատրաստի լուծույթի կայունությունից:
2 Որոշեք լուծման ծավալը, որը ցանկանում եք պատրաստել: Նյութի պահանջվող զանգվածը պարզելու համար նախ պետք է որոշեք ձեզ անհրաժեշտ լուծույթի վերջնական ծավալը: Այս ծավալը կախված է նրանից, թե որքան լուծում է անհրաժեշտ, որքան հաճախ եք այն օգտագործելու և պատրաստի լուծույթի կայունությունից: - Եթե Ձեզ անհրաժեշտ է ամեն անգամ օգտագործել թարմ լուծում, պատրաստեք միայն այն գումարը, որն անհրաժեշտ է մեկ օգտագործման համար:
- Եթե լուծումը երկար ժամանակ պահպանում է իր հատկությունները, կարող եք ավելի մեծ քանակությամբ պատրաստել այն հետագայում օգտագործելու համար:
- Օրինակ. Անհրաժեշտ է պատրաստել 5% NaCl լուծույթ `500 մլ ծավալով:
 3 Հաշվիր նյութի գրամերի քանակը, որն անհրաժեշտ է լուծումը պատրաստելու համար: Գրամների անհրաժեշտ քանակը հաշվարկելու համար օգտագործեք հետևյալ բանաձևը `գրամերի քանակ = (պահանջվում է տոկոս) (պահանջվող ծավալը / 100 մլ): Այս դեպքում պահանջվող տոկոսները արտահայտվում են գրամներով, իսկ պահանջվող ծավալը ՝ միլիլիտրերով:
3 Հաշվիր նյութի գրամերի քանակը, որն անհրաժեշտ է լուծումը պատրաստելու համար: Գրամների անհրաժեշտ քանակը հաշվարկելու համար օգտագործեք հետևյալ բանաձևը `գրամերի քանակ = (պահանջվում է տոկոս) (պահանջվող ծավալը / 100 մլ): Այս դեպքում պահանջվող տոկոսները արտահայտվում են գրամներով, իսկ պահանջվող ծավալը ՝ միլիլիտրերով: - Օրինակ ՝ Ձեզ անհրաժեշտ է պատրաստել 5% NaCl լուծույթ ՝ 500 մլ ծավալով:
- գրամների քանակ = (5 գ) (500 մլ / 100 մլ) = 25 գրամ:
- Եթե NaCl- ն տրվում է որպես լուծում, պարզապես վերցրեք 25 միլիլիտր NaCl գրամ փոշու փոխարեն և այդ ծավալը հանեք վերջնական ծավալից ՝ 25 միլիլիտր NaCl- ից մինչև 475 միլիլիտր ջուր:
 4 Քաշեք նյութը: Նյութի պահանջվող զանգվածը հաշվարկելուց հետո պետք է չափել այս գումարը: Վերցրեք չափագրված սանդղակ, դրա վրա դրեք աման և դրեք զրո: Կշռեք նյութի անհրաժեշտ քանակությունը գրամներով և թափեք այն:
4 Քաշեք նյութը: Նյութի պահանջվող զանգվածը հաշվարկելուց հետո պետք է չափել այս գումարը: Վերցրեք չափագրված սանդղակ, դրա վրա դրեք աման և դրեք զրո: Կշռեք նյութի անհրաժեշտ քանակությունը գրամներով և թափեք այն: - Նախքան լուծման պատրաստումը շարունակելը, համոզվեք, որ մաքրեք կշռող տապակը փոշու մնացորդներից:
- Վերոնշյալ օրինակում դուք պետք է կշռեք 25 գրամ NaCl:
 5 Լուծել նյութը անհրաժեշտ քանակությամբ հեղուկի մեջ: Եթե այլ բան նշված չէ, ջուրը օգտագործվում է որպես լուծիչ: Վերցրեք չափիչ բաժակ և չափեք անհրաժեշտ քանակությամբ հեղուկ: Այնուհետեւ փոշու նյութը լուծիր հեղուկի մեջ:
5 Լուծել նյութը անհրաժեշտ քանակությամբ հեղուկի մեջ: Եթե այլ բան նշված չէ, ջուրը օգտագործվում է որպես լուծիչ: Վերցրեք չափիչ բաժակ և չափեք անհրաժեշտ քանակությամբ հեղուկ: Այնուհետեւ փոշու նյութը լուծիր հեղուկի մեջ: - Ստորագրեք այն տարան, որի մեջ կպահեք լուծումը: Հստակ նշեք նյութը և դրա կոնցենտրացիան դրա վրա:
- Օրինակ `25 գրամ NaCl- ը լուծեք 500 միլիլիտր ջրի մեջ` 5% լուծույթ ստանալու համար:
- Հիշեք, որ եթե հեղուկ նյութ եք նոսրացնում, անհրաժեշտ քանակությամբ ջուր ստանալու համար լուծույթի վերջնական ծավալից հանեք ավելացված նյութի ծավալը ՝ 500 մլ - 25 մլ = 475 մլ ջուր:
Մեթոդ 2 4 -ից ՝ մոլեկուլային լուծույթի պատրաստում
 1 Որոշեք բանաձևի միջոցով օգտագործվող նյութի մոլեկուլային քաշը: Շշի պատին գրված է խառնուրդի բանաձևի քաշը (կամ պարզապես մոլեկուլային քաշը) գրամով մեկ մոլի համար (գ / մոլ): Եթե դուք չեք կարողանում գտնել շշի մոլեկուլային քաշը, նայեք առցանց:
1 Որոշեք բանաձևի միջոցով օգտագործվող նյութի մոլեկուլային քաշը: Շշի պատին գրված է խառնուրդի բանաձևի քաշը (կամ պարզապես մոլեկուլային քաշը) գրամով մեկ մոլի համար (գ / մոլ): Եթե դուք չեք կարողանում գտնել շշի մոլեկուլային քաշը, նայեք առցանց: - Նյութի մոլեկուլային քաշը այդ նյութի մեկ մոլի զանգվածն է (գրամներով):
- Օրինակ ՝ Նատրիումի քլորիդի (NaCl) մոլեկուլային քաշը 58,44 գ / մոլ է:
 2 Որոշեք պահանջվող լուծույթի ծավալը լիտրերով: Շատ հեշտ է պատրաստել մեկ լիտր լուծույթ, քանի որ դրա մոլարիտությունն արտահայտվում է մոլ / լիտրով, այնուամենայնիվ, գուցե անհրաժեշտ լինի ավելի կամ պակաս լիտր պատրաստել ՝ կախված լուծույթի նպատակից: Օգտագործեք վերջնական ծավալը `անհրաժեշտ քանակությամբ գրամ հաշվարկելու համար:
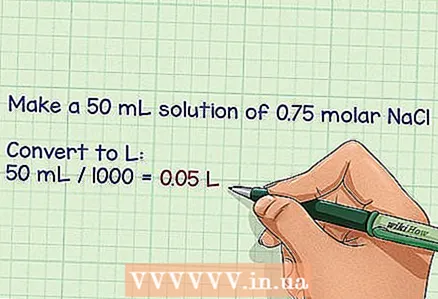
2 Որոշեք պահանջվող լուծույթի ծավալը լիտրերով: Շատ հեշտ է պատրաստել մեկ լիտր լուծույթ, քանի որ դրա մոլարիտությունն արտահայտվում է մոլ / լիտրով, այնուամենայնիվ, գուցե անհրաժեշտ լինի ավելի կամ պակաս լիտր պատրաստել ՝ կախված լուծույթի նպատակից: Օգտագործեք վերջնական ծավալը `անհրաժեշտ քանակությամբ գրամ հաշվարկելու համար: - Օրինակ. Անհրաժեշտ է պատրաստել 50 մլ լուծույթ `NaCl- ի 0,75 մոլային բաժնով:
- Միլիտրը լիտր դարձնելու համար դրանք բաժանեք 1000 -ի և ստացեք 0,05 լիտր:
 3 Հաշվիր պահանջվող մոլեկուլային լուծույթը պատրաստելու համար պահանջվող գրամների քանակը: Դա անելու համար օգտագործեք հետևյալ բանաձևը ՝ գրամների քանակ = (պահանջվող ծավալը) (պահանջվող մոլարայնություն) (մոլեկուլային քաշը ըստ բանաձևի): Հիշեք, որ պահանջվող ծավալը արտահայտվում է լիտրերով, մոլյարությունը `մոլ / լիտրով, իսկ մոլեկուլային քաշը ըստ բանաձևի` գրամ մեկ մոլի համար:
3 Հաշվիր պահանջվող մոլեկուլային լուծույթը պատրաստելու համար պահանջվող գրամների քանակը: Դա անելու համար օգտագործեք հետևյալ բանաձևը ՝ գրամների քանակ = (պահանջվող ծավալը) (պահանջվող մոլարայնություն) (մոլեկուլային քաշը ըստ բանաձևի): Հիշեք, որ պահանջվող ծավալը արտահայտվում է լիտրերով, մոլյարությունը `մոլ / լիտրով, իսկ մոլեկուլային քաշը ըստ բանաձևի` գրամ մեկ մոլի համար: - Օրինակ. Եթե ցանկանում եք պատրաստել 50 միլիլիտր լուծույթ NaCl 0,75 մոլային բաժնով (մոլեկուլային քաշը ըստ բանաձևի ՝ 58.44 գ / մոլ), ապա պետք է հաշվարկեք NaCl գրամների քանակը:
- գրամների քանակ = 0,05 լ * 0,75 մոլ / լ * 58,44 գ / մոլ = 2,19 գրամ NaCl:
- Չափման միավորները նվազեցնելով ՝ դուք ստանում եք գրամ նյութ:
 4 Քաշեք նյութը: Կշռեք պահանջվող գումարը `օգտագործելով ճիշտ ճշգրտված հաշվեկշիռ: Տեղադրեք մի գունդ հավասարակշռության վրա և զրոյից առաջ քաշելուց առաջ: Նյութը ավելացրեք ամանի մեջ մինչև հասնեք ցանկալի զանգվածի:
4 Քաշեք նյութը: Կշռեք պահանջվող գումարը `օգտագործելով ճիշտ ճշգրտված հաշվեկշիռ: Տեղադրեք մի գունդ հավասարակշռության վրա և զրոյից առաջ քաշելուց առաջ: Նյութը ավելացրեք ամանի մեջ մինչև հասնեք ցանկալի զանգվածի: - Օգտագործելուց հետո մաքրեք կշռող տապակը:
- Օրինակ ՝ կշռել 2.19 գրամ NaCl:
 5 Փոշը լուծարեք անհրաժեշտ քանակությամբ հեղուկի մեջ: Եթե այլ բան նշված չէ, լուծումների մեծ մասն օգտագործում է ջուր: Այս դեպքում վերցվում է հեղուկի նույն ծավալը, որն օգտագործվել է նյութի զանգվածը հաշվարկելու համար: Ավելացրեք նյութը ջրի մեջ և խառնեք մինչև ամբողջովին լուծարվի:
5 Փոշը լուծարեք անհրաժեշտ քանակությամբ հեղուկի մեջ: Եթե այլ բան նշված չէ, լուծումների մեծ մասն օգտագործում է ջուր: Այս դեպքում վերցվում է հեղուկի նույն ծավալը, որն օգտագործվել է նյութի զանգվածը հաշվարկելու համար: Ավելացրեք նյութը ջրի մեջ և խառնեք մինչև ամբողջովին լուծարվի: - Ստորագրեք կոնտեյները լուծույթով: Հստակ պիտակավորեք լուծված նյութը և մոլայնությունը, որպեսզի հետագայում կարողանաք օգտագործել լուծույթը:
- Օրինակ. Գավաթի (ծավալի չափման գործիք) միջոցով չափեք 50 մլ ջուր և դրա մեջ լուծեք 2,19 գրամ NaCl:
- Խառնել լուծումը մինչև փոշին ամբողջությամբ լուծարվի:
Մեթոդ 3 4 -ից. Հայտնի կոնցենտրացիայի լուծույթների լուծում
 1 Որոշեք յուրաքանչյուր լուծույթի կոնցենտրացիան: Լուծումները նոսրացնելիս պետք է իմանալ սկզբնական լուծույթի կոնցենտրացիան և այն լուծույթը, որը ցանկանում ես ստանալ:Այս մեթոդը հարմար է կենտրոնացված լուծույթները նոսրացնելու համար:
1 Որոշեք յուրաքանչյուր լուծույթի կոնցենտրացիան: Լուծումները նոսրացնելիս պետք է իմանալ սկզբնական լուծույթի կոնցենտրացիան և այն լուծույթը, որը ցանկանում ես ստանալ:Այս մեթոդը հարմար է կենտրոնացված լուծույթները նոսրացնելու համար: - Օրինակ `5 Մ լուծույթից պատրաստեք 75 միլիլիտր 1.5 Մ NaCl լուծույթ: Պահեստային լուծույթն ունի 5 Մ խտություն և անհրաժեշտ է այն նոսրացնել մինչև 1.5 Մ կոնցենտրացիայի:
 2 Որոշեք վերջնական լուծույթի ծավալը: Անհրաժեշտ է գտնել այն լուծման ծավալը, որը ցանկանում եք ստանալ: Դուք ստիպված կլինեք հաշվարկել լուծույթի այն քանակությունը, որը կպահանջվի այս լուծույթը ցանկալի կոնցենտրացիայի և ծավալի նոսրացնելու համար:
2 Որոշեք վերջնական լուծույթի ծավալը: Անհրաժեշտ է գտնել այն լուծման ծավալը, որը ցանկանում եք ստանալ: Դուք ստիպված կլինեք հաշվարկել լուծույթի այն քանակությունը, որը կպահանջվի այս լուծույթը ցանկալի կոնցենտրացիայի և ծավալի նոսրացնելու համար: - Օրինակ. Պատրաստեք 75 միլիլիտր 1.5 Մ NaCl լուծույթ նախնական 5 Մ լուծույթից: Այս օրինակում լուծույթի վերջնական ծավալը 75 միլիլիտր է:
 3 Հաշվիր սկզբնական լուծույթը նոսրացնելու համար անհրաժեշտ լուծույթի ծավալը: Դա անելու համար ձեզ հարկավոր է հետևյալ բանաձևը ՝ V1Գ1= Վ2Գ2որտեղ Վ1 - պահանջվող լուծույթի ծավալը, Գ1 - դրա համակենտրոնացումը, Վ2 - վերջնական լուծույթի ծավալը, Գ2 - նրա համակենտրոնացումը:
3 Հաշվիր սկզբնական լուծույթը նոսրացնելու համար անհրաժեշտ լուծույթի ծավալը: Դա անելու համար ձեզ հարկավոր է հետևյալ բանաձևը ՝ V1Գ1= Վ2Գ2որտեղ Վ1 - պահանջվող լուծույթի ծավալը, Գ1 - դրա համակենտրոնացումը, Վ2 - վերջնական լուծույթի ծավալը, Գ2 - նրա համակենտրոնացումը: - Պահանջվող հեղուկի ծավալը հաշվարկելու համար անհրաժեշտ է վերաշարադրել հավասարությունը V- ի նկատմամբ1: V1 = (Վ2Գ2) / Գ1.
- Օրինակ. Դուք պետք է պատրաստեք NaCl- ի 75 մլ լուծույթ ՝ 1.5 Մ կոնցենտրացիայով, 5 Մ կոնցենտրացիայի լուծույթից:
- Վ1 = (Վ2Գ2) / Գ1 = (0.075 լ * 1.5 Մ) / 5 Մ = 0.0225 լ:
- Լիտրերը դարձեք միլիլիտր ՝ բազմապատկելով 1000 -ով ՝ ստանալով 22,5 միլիլիտր:
 4 Նախնական լուծույթի ծավալը հանեք պլանավորված վերջնական ծավալից: Լուծույթի նոսրացման արդյունքում անհրաժեշտ է ձեռք բերել ֆիքսված վերջնական ծավալ: Վերջնական ծավալից հանեք պաշարների լուծույթի ծավալը `որոշելու լուծույթի լուծույթի ծավալը:
4 Նախնական լուծույթի ծավալը հանեք պլանավորված վերջնական ծավալից: Լուծույթի նոսրացման արդյունքում անհրաժեշտ է ձեռք բերել ֆիքսված վերջնական ծավալ: Վերջնական ծավալից հանեք պաշարների լուծույթի ծավալը `որոշելու լուծույթի լուծույթի ծավալը: - Օրինակ. Վերջնական ծավալը 75 միլիլիտր է, իսկ սկզբնական ծավալը `22.5 միլիլիտր: Այսպիսով, մենք ստանում ենք 75 - 22.5 = 52.5 միլիլիտր: Հեղուկի այս ծավալն է անհրաժեշտ լուծումը նոսրացնելու համար:
 5 Պահեստային լուծույթի հաշվարկված գումարը խառնել նոսրացման հեղուկի հետ: Օգտագործելով բաժակ (հեղուկի ծավալը չափելու գործիք), չափեք պաշարների լուծույթի անհրաժեշտ քանակությունը և խառնեք այն նոսրացման հեղուկի պահանջվող ծավալին:
5 Պահեստային լուծույթի հաշվարկված գումարը խառնել նոսրացման հեղուկի հետ: Օգտագործելով բաժակ (հեղուկի ծավալը չափելու գործիք), չափեք պաշարների լուծույթի անհրաժեշտ քանակությունը և խառնեք այն նոսրացման հեղուկի պահանջվող ծավալին: - Օրինակ. Չափել 5 Մ NaCl պաշարային լուծույթի 22.5 միլիլիտր և նոսրացնել 52.5 միլիլիտր ջրով: Խառնել լուծումը:
- Նոսրացված լուծույթով տարայի վրա գրեք դրա կոնցենտրացիան և կազմը ՝ 1.5 Մ NaCl:
- Հիշեք, եթե թթուն ջրով եք նոսրացնում, ապա պետք է թթու ավելացնեք ջրի մեջ, բայց ոչ հակառակը:
Մեթոդ 4 -ից 4 -ը. Համապատասխանություն անվտանգության նախազգուշական միջոցներին
 1 Օգտագործեք անձնական պաշտպանիչ սարքավորումներ: Ագրեսիվ քիմիական նյութերի և լուծույթների հետ աշխատելիս պաշտպանեք դրանց ազդեցությունից: Համոզվեք, որ հագեք լաբորատորիայի վերարկու, փակ կոշիկներ, անվտանգության ակնոցներ և ձեռնոցներ:
1 Օգտագործեք անձնական պաշտպանիչ սարքավորումներ: Ագրեսիվ քիմիական նյութերի և լուծույթների հետ աշխատելիս պաշտպանեք դրանց ազդեցությունից: Համոզվեք, որ հագեք լաբորատորիայի վերարկու, փակ կոշիկներ, անվտանգության ակնոցներ և ձեռնոցներ: - Օգտագործեք ոչ այրվող նյութից պատրաստված լաբորատոր վերարկու:
- Անվտանգության ակնոցները պետք է ունենան կողային վահաններ, որոնք ծածկում են աչքերը կողքից:
 2 Աշխատեք լավ օդափոխվող տարածքում: Երբ լուծումները խառնվում են, անկայուն գազերը կարող են ազատվել: Որոշ նյութեր պետք է մշակվեն միայն լաբորատոր կափարիչի տակ: Եթե դուք լուծումներ եք խառնում տանը, բացեք պատուհանները և միացրեք օդափոխիչը `օդի համապատասխան շրջանառություն ապահովելու համար:
2 Աշխատեք լավ օդափոխվող տարածքում: Երբ լուծումները խառնվում են, անկայուն գազերը կարող են ազատվել: Որոշ նյութեր պետք է մշակվեն միայն լաբորատոր կափարիչի տակ: Եթե դուք լուծումներ եք խառնում տանը, բացեք պատուհանները և միացրեք օդափոխիչը `օդի համապատասխան շրջանառություն ապահովելու համար:  3 Acidրի մեջ ավելացրեք թթու: Խիտ թթուները նոսրացնելիս միշտ թթուն ավելացրեք ջրի մեջ: Երբ ջուրն ու թթուն խառնվում են, տեղի է ունենում էկզոթերմիկ (ջերմության արտանետմամբ) ռեակցիա, որը թթվին ջուր ավելացնելու դեպքում կարող է հանգեցնել պայթյունի, և ոչ թե հակառակը:
3 Acidրի մեջ ավելացրեք թթու: Խիտ թթուները նոսրացնելիս միշտ թթուն ավելացրեք ջրի մեջ: Երբ ջուրն ու թթուն խառնվում են, տեղի է ունենում էկզոթերմիկ (ջերմության արտանետմամբ) ռեակցիա, որը թթվին ջուր ավելացնելու դեպքում կարող է հանգեցնել պայթյունի, և ոչ թե հակառակը: - Ամեն անգամ թթուների հետ աշխատելիս հիշեք անվտանգության նախազգուշական միջոցները:
Խորհուրդներ
- Նախքան սկսելը, ծանոթացեք թեմային: Գիտելիքը ուժ է:
- Փորձեք օգտագործել սովորական կենցաղային ապրանքներ: Մի փորձեք որեւէ արտառոց բան անել: Եթե կասկածում եք, որ վտանգ կարող է առաջանալ, հանձնվեք:
Գուշացումներ
- Մի խառնեք սպիտակեցնող նյութը և ամոնիակը:
- Անհրաժեշտության դեպքում օգտագործեք անվտանգության սարքավորումներ, ակնոցներ, պլաստմասե գոգնոց և նեոպրենային ձեռնոցներ:
Ինչ է պետք
- Mechanicalշգրիտ մեխանիկական կամ էլեկտրոնային կշեռքներ `զանգվածը որոշելու համար: Օրինակ, կարող եք օգտագործել խոհանոցի սանդղակ:
- Ավարտված ապակյա իրեր: Այս պարագաները կարելի է գտնել խոհանոցային սպասքի խանութում կամ պատվիրել առցանց: Չափիչ ապակին գալիս է տարբեր ձևերի և չափերի: Պլաստիկ սպասքը կաշխատի, չնայած նրանք չեն դիմանա բարձր ջերմաստիճաններին: