Հեղինակ:
Frank Hunt
Ստեղծման Ամսաթիվը:
16 Մարտ 2021
Թարմացման Ամսաթիվը:
27 Հունիս 2024

Բովանդակություն
- Քայլել
- 2-ի մեթոդ 1. Արագ կանոնների օգտագործում
- 2-ի մեթոդ 2. Կ – ի լուծելիության հաշվարկ:սպ
- Անհրաժեշտությունները
- Խորհուրդներ
- Arnգուշացումներ
Քիմիայում լուծելիությունն օգտագործվում է այն պինդ նյութի հատկությունները նկարագրելու համար, որը խառնվում է և ամբողջությամբ լուծվում է հեղուկի մեջ ՝ չթողնելով չլուծված մասնիկներ: Լուծվում են միայն (լիցքավորված) իոնային միացությունները: Գործնական նպատակներով, մի քանի կանոն մտապահելը կամ կանոնների ցանկը խորհրդակցելը բավական է ձեզ ասելու, թե իոնային միացությունների մեծ մասը ջրի հետ խառնվելիս պինդ կմնա՞ն, թե՞ զգալի քանակությամբ լուծարվում է: Իրականում, որոշ մոլեկուլներ կլուծվեն, նույնիսկ եթե փոփոխություններ չես տեսնում, այնպես որ ճշգրիտ փորձերի համար հարկավոր է իմանալ, թե ինչպես հաշվարկել այդ գումարը:
Քայլել
2-ի մեթոդ 1. Արագ կանոնների օգտագործում
 Իմացեք ավելին իոնային միացությունների մասին: Յուրաքանչյուր ատոմ սովորաբար ունենում է մի շարք էլեկտրոններ, բայց երբեմն նրանք ձեռք են բերում կամ կորցնում են մեկ լրացուցիչ էլեկտրոն: Արդյունքը մեկն է իոն էլեկտրական լիցքով: Երբ բացասական լիցք ունեցող իոնը (լրացուցիչ էլեկտրոն) հանդիպում է դրական լիցքով իոնին (էլեկտրոնը բացակայում է), դրանք միանում են իրար, ճիշտ այնպես, ինչպես երկու մագնիսների բացասական և դրական ծայրերը: Արդյունքն իոնային կապ է:
Իմացեք ավելին իոնային միացությունների մասին: Յուրաքանչյուր ատոմ սովորաբար ունենում է մի շարք էլեկտրոններ, բայց երբեմն նրանք ձեռք են բերում կամ կորցնում են մեկ լրացուցիչ էլեկտրոն: Արդյունքը մեկն է իոն էլեկտրական լիցքով: Երբ բացասական լիցք ունեցող իոնը (լրացուցիչ էլեկտրոն) հանդիպում է դրական լիցքով իոնին (էլեկտրոնը բացակայում է), դրանք միանում են իրար, ճիշտ այնպես, ինչպես երկու մագնիսների բացասական և դրական ծայրերը: Արդյունքն իոնային կապ է: - Կոչվում են բացասական լիցք ունեցող իոններ անիոններ, և իոնները ՝ դրական լիցքով կատիոններ.
- Սովորաբար, ատոմի էլեկտրոնների քանակը հավասար է պրոտոնների քանակին, որտեղ էլեկտրական լիցքերը հավասարակշռության մեջ են:
 Իմացեք լուծելիությունը: Molecրի մոլեկուլներ (Հ.2Ո) ունեն անսովոր կառուցվածք, որով նրանք իրենց մագնիսի պես են պահում. Մի ծայրն ունի դրական լիցք, իսկ մյուս ծայրը ՝ բացասական: Երբ իոնային կապը ջրի հետ խառնեք, այդ «ջրային մագնիսները» կհավաքվեն դրա շուրջ ՝ փորձելով տարանջատել դրական և բացասական իոնները: Իոնային որոշ կապեր իրար շատ ամուր չեն. Սրանք լուծելիքանի որ ջուրը կպատռի և կլուծարի կապը: Այլ կոմպոզիտորներն ունեն ավելի ամուր կապեր և կան Լուծվող չէքանի որ նրանք կարող են միասին մնալ չնայած ջրի մոլեկուլներին:
Իմացեք լուծելիությունը: Molecրի մոլեկուլներ (Հ.2Ո) ունեն անսովոր կառուցվածք, որով նրանք իրենց մագնիսի պես են պահում. Մի ծայրն ունի դրական լիցք, իսկ մյուս ծայրը ՝ բացասական: Երբ իոնային կապը ջրի հետ խառնեք, այդ «ջրային մագնիսները» կհավաքվեն դրա շուրջ ՝ փորձելով տարանջատել դրական և բացասական իոնները: Իոնային որոշ կապեր իրար շատ ամուր չեն. Սրանք լուծելիքանի որ ջուրը կպատռի և կլուծարի կապը: Այլ կոմպոզիտորներն ունեն ավելի ամուր կապեր և կան Լուծվող չէքանի որ նրանք կարող են միասին մնալ չնայած ջրի մոլեկուլներին: - Որոշ կապեր ունեն ներքին կապեր, որոնք ուժով համեմատելի են ջրի ձգման հետ: Այս նյութերն են չափավոր լուծելի, քանի որ պարտատոմսերի զգալի մասը (բայց ոչ բոլորը) կտարվեն:
 Ուսումնասիրեք լուծելիության կանոնները: Քանի որ ատոմների փոխազդեցությունը բավականին բարդ է, միշտ չէ, որ ինտուիտիվ է, թե որ միացությունները են լուծելի և անլուծելի: Ստորև բերված ցուցակում գտեք բարդ առաջին բաղադրիչը ՝ պարզելու համար, թե ինչպես է այն սովորաբար վարվում, ապա ստուգեք բացառությունները ՝ համոզվելու համար, որ երկրորդ իոնն աննորմալ չի փոխազդում:
Ուսումնասիրեք լուծելիության կանոնները: Քանի որ ատոմների փոխազդեցությունը բավականին բարդ է, միշտ չէ, որ ինտուիտիվ է, թե որ միացությունները են լուծելի և անլուծելի: Ստորև բերված ցուցակում գտեք բարդ առաջին բաղադրիչը ՝ պարզելու համար, թե ինչպես է այն սովորաբար վարվում, ապա ստուգեք բացառությունները ՝ համոզվելու համար, որ երկրորդ իոնն աննորմալ չի փոխազդում: - Օրինակ ՝ օգտագործել ստրոնցիումի քլորիդ (SrCl)2), որոնեք Sr կամ Cl ստորև նշված համարձակ քայլերով: Cl- ը «հիմնականում լուծելի է», ուստի ստուգեք բացառությունները ստորև: Sr- ը որպես բացառություն նշված չէ, ուստի SrCl2 լինել լուծելի:
- Ստորև բերված են յուրաքանչյուր կանոնի ամենատարածված բացառությունները: Կան այլ բացառություններ, բայց դրանք, հավանաբար, չեք գտնի քիմիայի ընդհանուր դասարանում կամ լաբորատորիայում:
 Բարդությունները լուծելի են, երբ դրանք պարունակում են ալկալային մետաղներ, այդ թվում `Li, Na, K, Rb և C: Դրանք նաև կոչվում են IA խմբի տարրեր ՝ լիթիում, նատրիում, կալիում, ռուբիդիում և ցեզիում: Այս իոններից որևէ մեկը պարունակող գրեթե ցանկացած բաղադրություն լուծելի է:
Բարդությունները լուծելի են, երբ դրանք պարունակում են ալկալային մետաղներ, այդ թվում `Li, Na, K, Rb և C: Դրանք նաև կոչվում են IA խմբի տարրեր ՝ լիթիում, նատրիում, կալիում, ռուբիդիում և ցեզիում: Այս իոններից որևէ մեկը պարունակող գրեթե ցանկացած բաղադրություն լուծելի է: - Բացառություն: Լի3PO4 լուծելի չէ:
 Միացություններ ՈՉ-ով3, Գ2Հ.3Ո2, ՈՉ2, ClO3 և ClO- ն4 լուծելի են: Սրանք համապատասխանաբար նիտրատի, ացետատի, նիտրիտի, քլորատի և պերքլորատի իոններն են: Նշենք, որ ացետատը հաճախ կրճատվում է OAc- ով:
Միացություններ ՈՉ-ով3, Գ2Հ.3Ո2, ՈՉ2, ClO3 և ClO- ն4 լուծելի են: Սրանք համապատասխանաբար նիտրատի, ացետատի, նիտրիտի, քլորատի և պերքլորատի իոններն են: Նշենք, որ ացետատը հաճախ կրճատվում է OAc- ով: - Բացառություններ. Ag (OAc) (արծաթի ացետատ) և Hg (OAc)2 (սնդիկի ացետատ) լուծելի չեն:
- AgNO2 և KClO4 միայն «մասամբ լուծելի» են:
 Cl, Br և I խառնուրդները սովորաբար լուծելի են: Քլորիդի, բրոմիդի և յոդիդի իոնները գրեթե միշտ կազմում են լուծվող միացություններ, որոնք հայտնի են նաև որպես հալոգենային աղեր:
Cl, Br և I խառնուրդները սովորաբար լուծելի են: Քլորիդի, բրոմիդի և յոդիդի իոնները գրեթե միշտ կազմում են լուծվող միացություններ, որոնք հայտնի են նաև որպես հալոգենային աղեր: - Բացառություն: Եթե դրանցից որևէ մեկը կապվում է արծաթի իոնների (Ag), սնդիկի (Hg) հետ2), կամ կապար (Pb), արդյունքը լուծելի չէ: Նույնը վերաբերում է պղնձի (Cu) և թալիումի (Tl) հետ քիչ տարածված միացություններին:
 Կապեր SO- ի հետ4 սովորաբար լուծելի են: Սուլֆատ իոնը սովորաբար կազմում է լուծվող միացություններ, բայց կան մի քանի բացառություններ:
Կապեր SO- ի հետ4 սովորաբար լուծելի են: Սուլֆատ իոնը սովորաբար կազմում է լուծվող միացություններ, բայց կան մի քանի բացառություններ: - Բացառություններ. Սուլֆատ իոնն անլուծելի միացություններ է առաջացնում հետևյալ իոններով. Ստրոնցիում Sr, բարիում Ba, կապարի Pb, արծաթ Ag, կալցիում Ca, ռադիում Ra և դիատոմիկ արծաթ Ag2, Նկատի ունեցեք, որ արծաթի սուլֆատը և կալցիումի սուլֆատը լուծվում են այնքան, որ երբեմն անվանում են թույլ լուծելի:
 OH կամ S– ի հետ միացությունները լուծելի չեն: Սրանք համապատասխանաբար հիդրօքսիդի և սուլֆիդի իոններն են:
OH կամ S– ի հետ միացությունները լուծելի չեն: Սրանք համապատասխանաբար հիդրօքսիդի և սուլֆիդի իոններն են: - Բացառություններ. Հիշու՞մ եք ալկալային մետաղները (I-A խումբ) և որքանո՞վ են նրանք սիրում լուծել չլուծվող միացություններ: Li, Na, K, Rb և Cs բոլորը կազմում են լուծվող միացություններ հիդրօքսիդի կամ սուլֆիդի իոններով: Բացի այդ, հիդրօքսիդը լուծելի աղեր է առաջացնում ալկալային հողի մետաղների (II-A խմբի) իոններով ՝ կալցիում Ca, ստրոնցիում Sr և բարիում Ba: Ուշադրություն դարձրեք, որ ալկալային հողի խառնուրդով հիդրօքսիդը բավականաչափ մոլեկուլներ ունի իրար կպցնելու համար, որպեսզի երբեմն համարվի «քիչ լուծելի»:
 Բաղադրիչներ CO- ով3 կամ PO4 լուծելի չեն: Վերջին անգամ ստուգեք կարբոնատային և ֆոսֆատային իոնների առկայությունը, և դուք պետք է իմանաք, թե ինչ կարելի է սպասել միացությունից:
Բաղադրիչներ CO- ով3 կամ PO4 լուծելի չեն: Վերջին անգամ ստուգեք կարբոնատային և ֆոսֆատային իոնների առկայությունը, և դուք պետք է իմանաք, թե ինչ կարելի է սպասել միացությունից: - Բացառություններ. Այս իոնները լուծվող միացություններ են ստեղծում սովորական նյութերով ՝ Li, Na, K, Rb և C ալկալային մետաղներով, ինչպես նաև NH ամոնիումով:4.
2-ի մեթոդ 2. Կ – ի լուծելիության հաշվարկ:սպ
 Փնտրեք կայուն Կ – ի լուծելիության արտադրանքը:սպ. Այս հաստատունը յուրաքանչյուր կապի համար տարբեր է, ուստի հարկ կլինի այն փնտրել ձեր դասագրքի կամ առցանց սեղանի մեջ: Քանի որ այդ արժեքները որոշվում են փորձնականորեն, դրանք կարող են մեծապես տարբեր լինել սեղանից սեղան, ուստի ամենալավն այն է, որ սեղանն օգտագործվի ձեր դասագրքում, եթե կա: Եթե այլ բան նշված չէ, սեղանների մեծ մասը ենթադրում է 25o C միջավայրի ջերմաստիճան:
Փնտրեք կայուն Կ – ի լուծելիության արտադրանքը:սպ. Այս հաստատունը յուրաքանչյուր կապի համար տարբեր է, ուստի հարկ կլինի այն փնտրել ձեր դասագրքի կամ առցանց սեղանի մեջ: Քանի որ այդ արժեքները որոշվում են փորձնականորեն, դրանք կարող են մեծապես տարբեր լինել սեղանից սեղան, ուստի ամենալավն այն է, որ սեղանն օգտագործվի ձեր դասագրքում, եթե կա: Եթե այլ բան նշված չէ, սեղանների մեծ մասը ենթադրում է 25o C միջավայրի ջերմաստիճան: - Օրինակ, եթե ցանկանում եք լուծարել կապարի յոդդը (PbI)2), գրի՛ր լուծվող արտադրանքի հավասարակշռության հաստատունը: Եթե bilbo.chm.uri.edu- ում աղյուսակ եք օգտագործում, օգտագործեք 7,1 × 10 հաստատունը:
 Նախ գրեք քիմիական հավասարումը: Նախ որոշեք, թե ինչպես է լուծույթը լուծվում, երբ բաղադրությունը բաժանվում է իոնների: Հիմա հավասարություն գրիր Կ.սպ մի կողմից, իսկ անհատական իոնները ՝ մյուս կողմից:
Նախ գրեք քիմիական հավասարումը: Նախ որոշեք, թե ինչպես է լուծույթը լուծվում, երբ բաղադրությունը բաժանվում է իոնների: Հիմա հավասարություն գրիր Կ.սպ մի կողմից, իսկ անհատական իոնները ՝ մյուս կողմից: - Օրինակ ՝ PbI մոլեկուլ2 բաժանվում է Pb, I և մեկ I իոնների մեջ (պետք է միայն իմանալ կամ փնտրել մեկ իոնի լիցքը, քանի որ գիտես, որ ընդհանուր բաղադրությունը միշտ ունի չեզոք լիցք):
- Գրիր 7.1 × 10 = [Pb] [I] հավասարումը
 Կարգավորեք հավասարումը ՝ փոփոխականներ օգտագործելու համար: Վերահաշվարկը վերաշարադրեք որպես հանրահաշվի միակ խնդիր ՝ օգտագործելով մոլեկուլների կամ իոնների քանակի վերաբերյալ ձեր գիտելիքները: Սահմանել x հավասար լուծվող նյութի քանակին և վերափոխել փոփոխականները որպես յուրաքանչյուր իոնի համարներ x- ի:
Կարգավորեք հավասարումը ՝ փոփոխականներ օգտագործելու համար: Վերահաշվարկը վերաշարադրեք որպես հանրահաշվի միակ խնդիր ՝ օգտագործելով մոլեկուլների կամ իոնների քանակի վերաբերյալ ձեր գիտելիքները: Սահմանել x հավասար լուծվող նյութի քանակին և վերափոխել փոփոխականները որպես յուրաքանչյուր իոնի համարներ x- ի: - Մեր օրինակում մենք վերաշարադրում ենք 7.1 × 10 = [Pb] [I]
- Քանի որ բաղադրության մեջ կա միայն մեկ կապարի իոն (Pb), լուծարված միացության մոլեկուլների քանակը հավասար կլինի ազատ կապարի իոնների քանակին: Այսպիսով, մենք կարող ենք [Pb] - ը փոխարինել x- ով:
- Քանի որ յուրաքանչյուր կապարի իոնի համար կա յոդի երկու իոն (I), մենք կարող ենք յոդի ատոմների քանակը հավասարեցնել 2x- ի:
- Հավասարությունն այժմ կարդում է 7.1 × 10 = (x) (2x)
 Հաշվի առեք սովորական իոնները, եթե այդպիսիք կան: Բաց թողեք այս քայլը, եթե լուծույթը լուծում եք մաքուր ջրի մեջ: Այնուամենայնիվ, եթե միացությունը լուծարվում է լուծույթում, որն արդեն պարունակում է մեկ կամ մի քանի բաղադրիչ իոններ («ընդհանուր իոն»), լուծելիությունը զգալիորեն կրճատվում է: Ընդհանուր իոնների ազդեցությունն առավել նկատելի է հիմնականում չլուծվող միացությունների մեջ, և այս դեպքերում կարելի է ենթադրել, որ հավասարակշռության իոնների ճնշող մեծամասնությունը գալիս է լուծույթում արդեն առկա իոնից: Հավասարը վերաշարադրեք արդեն լուծույթում պարունակվող իոնների հայտնի մոլային կոնցենտրացիայով (մոլ / լիտր կամ Մ) `փոխարինելով այդ իոնի համար օգտագործած x- ի արժեքը:
Հաշվի առեք սովորական իոնները, եթե այդպիսիք կան: Բաց թողեք այս քայլը, եթե լուծույթը լուծում եք մաքուր ջրի մեջ: Այնուամենայնիվ, եթե միացությունը լուծարվում է լուծույթում, որն արդեն պարունակում է մեկ կամ մի քանի բաղադրիչ իոններ («ընդհանուր իոն»), լուծելիությունը զգալիորեն կրճատվում է: Ընդհանուր իոնների ազդեցությունն առավել նկատելի է հիմնականում չլուծվող միացությունների մեջ, և այս դեպքերում կարելի է ենթադրել, որ հավասարակշռության իոնների ճնշող մեծամասնությունը գալիս է լուծույթում արդեն առկա իոնից: Հավասարը վերաշարադրեք արդեն լուծույթում պարունակվող իոնների հայտնի մոլային կոնցենտրացիայով (մոլ / լիտր կամ Մ) `փոխարինելով այդ իոնի համար օգտագործած x- ի արժեքը: - Օրինակ, եթե մեր կապարի-յոդի միացությունը լուծարվում էր 0.2 Մ կապարի քլորիդ պարունակող լուծույթի մեջ (PbCl)2), ապա կարող ենք հավասարումը վերաշարադրել որպես 7.1 × 10 = (0.2M + x) (2x): Եվ հետո, քանի որ 0.2M- ն x- ից բարձր կոնցենտրացիան է, մենք կարող ենք ապահով կերպով այն վերաշարադրել որպես 7.1 × 10 = (0.2M) (2x):
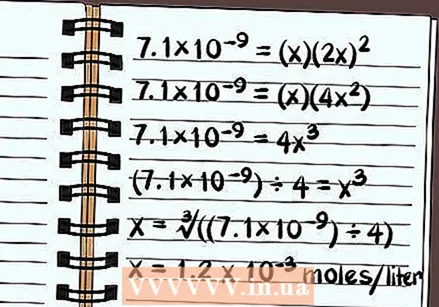 Լուծիր հավասարումը: Լուծեք x- ի համար և իմացեք, թե որքան լուծելի է բաղադրությունը: Լուծելիության հաստատունը որոշելու եղանակի պատճառով ձեր պատասխանը կարտահայտվի որպես լուծվող բաղադրության մոլերի քանակը մեկ լիտր ջրի համար: Գուցե ձեզ անհրաժեշտ լինի հաշվիչ `վերջնական պատասխանը գտնելու համար:
Լուծիր հավասարումը: Լուծեք x- ի համար և իմացեք, թե որքան լուծելի է բաղադրությունը: Լուծելիության հաստատունը որոշելու եղանակի պատճառով ձեր պատասխանը կարտահայտվի որպես լուծվող բաղադրության մոլերի քանակը մեկ լիտր ջրի համար: Գուցե ձեզ անհրաժեշտ լինի հաշվիչ `վերջնական պատասխանը գտնելու համար: - Հետևյալը վերաբերում է մաքուր ջրի լուծելիությանը, այլ ոչ թե ընդհանուր իոններով:
- 7.1 × 10 = (x) (2x)
- 7.1 × 10 = (x) (4x)
- 7.1 × 10 = 4x
- (7.1 × 10) ÷ 4 = x
- x = ∛ ((7.1 × 10) ÷ 4)
- x = Մեկ լիտրի համար 1,2 x 10 մոլը կլուծարվի, Սա շատ փոքր քանակ է, ուստի գիտեք, որ այս բաղադրությունը սկզբունքորեն թույլ լուծելի է:
Անհրաժեշտությունները
- Լուծունակության արտադրանքի հաստատունների աղյուսակ (Կ.սպ) միացումների համար:
Խորհուրդներ
- Եթե ունեք փորձեր ստացված տվյալներից, թե ինչ աստիճանի է լուծվում միացությունը, ապա կարող եք օգտագործել նույն հավասարումը լուծելիության հաստատունը Kսպ.
Arnգուշացումներ
- Այս տերմինների համընդհանուր ընդունված սահմանում գոյություն չունի, բայց քիմիկոսները համաձայն են միացությունների մեծամասնության վերաբերյալ: Լուծված և չլուծված մոլեկուլների զգալի համամասնությամբ միացությունների հետ կապված որոշ սահմանային դեպքեր կարելի է նկարագրել տարբեր լուծելիության աղյուսակներով:
- Որոշ հին դասագրքեր տալիս են NH4OH կրկին որպես լուծվող բաղադրություն: Սա սխալ է. փոքր քանակությամբ NH4 և OH իոնները կարող են դիտվել, բայց չեն կարող մեկուսացվել ՝ կազմելով բարդ: