Հեղինակ:
Christy White
Ստեղծման Ամսաթիվը:
8 Մայիս 2021
Թարմացման Ամսաթիվը:
1 Հուլիս 2024
Բովանդակություն
- Քայլել
- 3-ի մեթոդը 1-ին մաս. Առաջին մաս. Հասկանալով էլեկտրոնային թաղանթները
- 3-ի մեթոդը 2-րդ մաս. Երկրորդ մաս. Վալանսային էլեկտրոններ գտնել մետաղներում, բացառությամբ անցումային մետաղների
- 3-ի մեթոդը 3. Մաս Երրորդ. Վալանսային էլեկտրոններ գտնել անցումային մետաղներում
- Խորհուրդներ
- Անհրաժեշտությունները
Վալանսային էլեկտրոնները ընկած են տարրի արտաքին պատյանում: Ատոմում վալենտային էլեկտրոնների քանակը որոշում է այս տարրը կարող է առաջացնել քիմիական կապի տեսակը: Վալենտային էլեկտրոնների քանակը պարզելու լավագույն միջոցը տարրերի պարբերական աղյուսակն օգտագործելն է:
Քայլել
3-ի մեթոդը 1-ին մաս. Առաջին մաս. Հասկանալով էլեկտրոնային թաղանթները
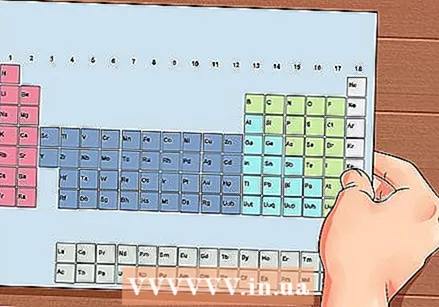 Տարրերի պարբերական աղյուսակ: Սա աղյուսակ է գունային ծածկագրերով, որտեղ յուրաքանչյուր բջիջում տարր է ցուցադրվում ատոմային թվով և 1-ից 3 տառերով `որպես խորհրդանիշ:
Տարրերի պարբերական աղյուսակ: Սա աղյուսակ է գունային ծածկագրերով, որտեղ յուրաքանչյուր բջիջում տարր է ցուցադրվում ատոմային թվով և 1-ից 3 տառերով `որպես խորհրդանիշ: 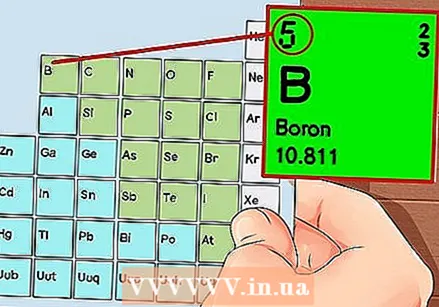 Գտեք տարրի ատոմային թիվը: Ատոմային համարը վեր է կամ տարրի խորհրդանիշի կողքին: Օրինակ ՝ Բորը (B) ունի 5 ատոմային համար, ինչը նշանակում է, որ այն ունի 5 պրոտոն և 5 էլեկտրոն:
Գտեք տարրի ատոմային թիվը: Ատոմային համարը վեր է կամ տարրի խորհրդանիշի կողքին: Օրինակ ՝ Բորը (B) ունի 5 ատոմային համար, ինչը նշանակում է, որ այն ունի 5 պրոտոն և 5 էլեկտրոն: 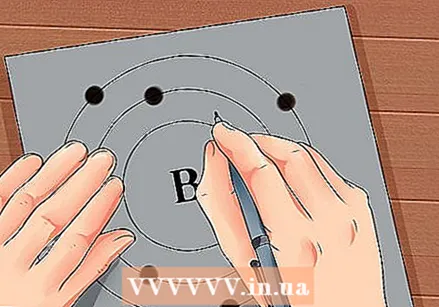 Նկարեք ատոմի պարզ ներկայացում և էլեկտրոնները տեղադրեք ուղեծրի միջուկի շուրջ: Այս աշխատանքները կոչվում են նաև խեցիներ կամ էներգիայի մակարդակներ: Էլեկտրոնների առավելագույն քանակը, որոնք կարող են լինել նույն թաղանթում, ամրագրված է, և թաղանթները լցվում են ներքինից դեպի արտաքին ուղեծիր:
Նկարեք ատոմի պարզ ներկայացում և էլեկտրոնները տեղադրեք ուղեծրի միջուկի շուրջ: Այս աշխատանքները կոչվում են նաև խեցիներ կամ էներգիայի մակարդակներ: Էլեկտրոնների առավելագույն քանակը, որոնք կարող են լինել նույն թաղանթում, ամրագրված է, և թաղանթները լցվում են ներքինից դեպի արտաքին ուղեծիր: - K Shell (ներքին) ՝ առավելագույնը 2 էլեկտրոն:
- L Shell: առավելագույնը 8 էլեկտրոն:
- M Shell ՝ առավելագույնը 18 էլեկտրոն:
- N Shell ՝ առավելագույնը 32 էլեկտրոն:
- O Shell ՝ առավելագույնը 50 էլեկտրոն:
- P Shell (արտաքին) ՝ առավելագույնը 72 էլեկտրոն:
 Գտեք արտաքին թաղանթի էլեկտրոնների քանակը: Սրանք վալենտային էլեկտրոններ են:
Գտեք արտաքին թաղանթի էլեկտրոնների քանակը: Սրանք վալենտային էլեկտրոններ են: - Երբ վալենտային կեղևը լրիվ է, տարրը կայուն է:
- Եթե վալենտային թաղանթը լրիվ չէ, ապա տարրը ռեակտիվ է, ինչը նշանակում է, որ այն կարող է քիմիապես կապվել մեկ այլ տարրի ատոմի հետ: Յուրաքանչյուր ատոմ կիսում է իր վալենտային էլեկտրոնները ՝ փորձելով վալենտային կեղևը լիարժեք դարձնել:
3-ի մեթոդը 2-րդ մաս. Երկրորդ մաս. Վալանսային էլեկտրոններ գտնել մետաղներում, բացառությամբ անցումային մետաղների
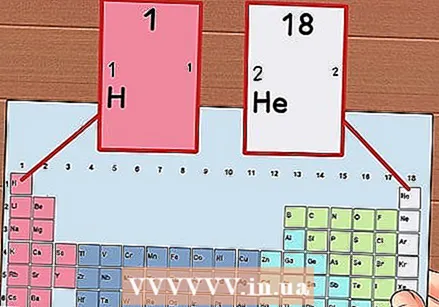 Համարեք պարբերական աղյուսակի յուրաքանչյուր սյունակ `1-ից 18: Hydրածինը (H) սյունակի 1-ին վերին մասում է, իսկ Հելիումը (Նա) `18-րդ սյունակի վերևում: Սրանք տարրերի տարբեր խմբերն են:
Համարեք պարբերական աղյուսակի յուրաքանչյուր սյունակ `1-ից 18: Hydրածինը (H) սյունակի 1-ին վերին մասում է, իսկ Հելիումը (Նա) `18-րդ սյունակի վերևում: Սրանք տարրերի տարբեր խմբերն են: 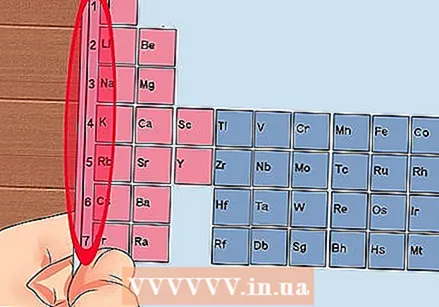 Յուրաքանչյուր շարքին տվեք թիվ `1-ից 7-ը: Սրանք տարրերի ժամանակաշրջաններ են, և դրանք համապատասխանում են ատոմի կեղևների քանակին կամ էներգիայի մակարդակներին:
Յուրաքանչյուր շարքին տվեք թիվ `1-ից 7-ը: Սրանք տարրերի ժամանակաշրջաններ են, և դրանք համապատասխանում են ատոմի կեղևների քանակին կամ էներգիայի մակարդակներին: - Hydրածին (H) և հելիում (He) երկուսն էլ ունեն 1 թաղանթ, մինչդեռ Francium (Fr) 7:
- Լանտանիդները և ակտինիդները խմբավորված են և նշված են հիմնական աղյուսակի տակ: Բոլոր lanthanides- ը պատկանում է 6-րդ ժամանակաշրջանին, 3-րդ խումբին, և բոլոր ակտինիդները պատկանում են 7-րդ Period- ին, 3-րդ խմբին:
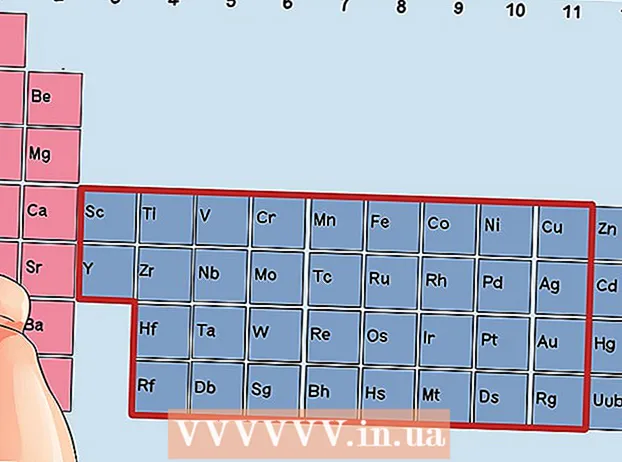
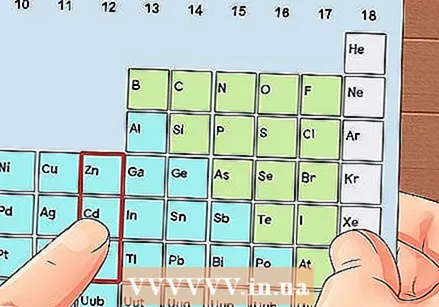 Գտեք այն տարրը, որը անցումային մետաղ չէ: Անցումային մետաղները գտնվում են 3-ից 12-րդ խմբերի մեջ: Մյուս մետաղների խմբային համարները նշում են վալենտային էլեկտրոնների քանակը:
Գտեք այն տարրը, որը անցումային մետաղ չէ: Անցումային մետաղները գտնվում են 3-ից 12-րդ խմբերի մեջ: Մյուս մետաղների խմբային համարները նշում են վալենտային էլեկտրոնների քանակը: - Խումբ 1: 1 վալենտային էլեկտրոն
- Խումբ 2. 2 վալենտային էլեկտրոն
- 13-րդ խումբ. 3 վալենտային էլեկտրոն
- 14-րդ խումբ. 4 վալենտային էլեկտրոն
- 15-րդ խումբ. 5 վալենտային էլեկտրոն
- 16-րդ խումբ ՝ 6 վալենտային էլեկտրոն
- 17-րդ խումբ. 7 վալենտային էլեկտրոն
- 18-րդ խումբ. 8 վալենտային էլեկտրոններ `բացառությամբ Հելիումի, որն ունի 2
3-ի մեթոդը 3. Մաս Երրորդ. Վալանսային էլեկտրոններ գտնել անցումային մետաղներում
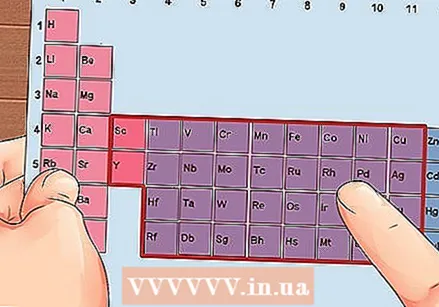 Գտեք 3-ից 12-րդ խմբի տարր `անցումային մետաղները:
Գտեք 3-ից 12-րդ խմբի տարր `անցումային մետաղները: Որոշեք վալենտային էլեկտրոնների քանակը `ելնելով խմբի համարից: Այս խմբի համարները համապատասխանում են վալենտային էլեկտրոնների հնարավոր թվին:
Որոշեք վալենտային էլեկտրոնների քանակը `ելնելով խմբի համարից: Այս խմբի համարները համապատասխանում են վալենտային էլեկտրոնների հնարավոր թվին: - Խումբ 3. 3 վալենտային էլեկտրոն
- 4-րդ խումբ. 2-ից 4 վալենտային էլեկտրոններ
- Խումբ 5` 2-ից 5 վալենտային էլեկտրոն
- 6-րդ խումբ. 2-ից 6 վալենտային էլեկտրոններ
- 7-րդ խումբ. 2-ից 7 վալենտային էլեկտրոններ
- 8-րդ խումբ. 2 կամ 3 վալենտային էլեկտրոններ
- 9-րդ խումբ. 2 կամ 3 վալենտային էլեկտրոններ
- 10. խումբ ՝ 2 կամ 3 վալենտային էլեկտրոններ
- 11-րդ խումբ. 1 կամ 2 վալենտային էլեկտրոններ
- 12-րդ խումբ. 2 վալենտային էլեկտրոն
Խորհուրդներ
- Անցումային մետաղները կարող են ունենալ վալենտային թաղանթներ, որոնք ամբողջությամբ լի չեն: Անցումային մետաղներում վալենտային էլեկտրոնների ճշգրիտ քանակի որոշումը պահանջում է քվանտային տեսության որոշակի սկզբունքներ, որոնք դուրս են սույն հոդվածի շրջանակից:
Անհրաժեշտությունները
- Տարրերի պարբերական աղյուսակ
- Մատիտ
- Թուղթ